Los gases reales, también conocidos como gases no ideales, son aquellos que presentan desviaciones al comportamiento de un gas ideal. Esta diferencia de comportamiento se debe principalmente a las interacciones entre las moléculas del gas.
 |
| Fuga de gas de una toma manométrica. Imagen de plumbingandelectrical |
En condiciones de producción industrial, la mayoría de los gases son reales debido a que el modelo de gas ideal se utiliza para simplificar los cálculos tomando diversas consideraciones, siendo la más importante, las presiones bajas de operación.
Comúnmente nos encontramos a nivel industrial con presiones moderadas o altas, lo que impide utilizar el modelo de gas ideal para estimar propiedades, es por ello, que el concepto de gas real es tan importante para la ingeniería.
En este artículo, definiremos al gas real, el comportamiento del gas real, el factor de compresibilidad de un gas y cómo estimarlo.
Tabla de contenidos
- ✔Definición de gas real o gas no ideal
- ✔Comportamiento de un gas real o no ideal
- ✔¿Cuándo difiere un gas real de un gas ideal?
- ✔Factor de compresibilidad de un gas (Z)
Definición de gas real o gas no ideal
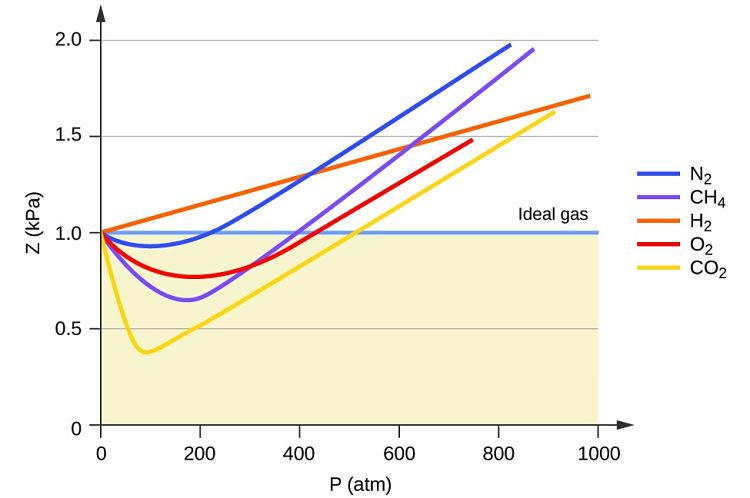 |
| Desviaciones de la idealidad de algunos gases. Imagen de courseslumenlearning |
En la termodinámica el estudio de los gases es muy común y para simplificar los cálculos se utiliza el modelo de gas ideal, sólo si las presiones a las cuales se estudia el gas fuesen presiones bajas (algunos autores recomiendan presiones de hasta 5 atmósferas, otros hasta 10 atmósferas), e incluso, a temperaturas bajas. Para efectos prácticos y a nivel industrial, las condiciones de operación se desvían bastante de esta idealidad, es por esta razón, que es importante el conocimiento del gas con el que se trabaja o estudia, ya que su propia naturaleza lo desvía de las condiciones de idealidad.
Conociendo que la desviación del comportamiento de un gas ideal, es lo que define a un gas real, podemos decir lo siguiente:
Un gas no ideal o gas real, es aquel que presenta un comportamiento termodinámico particular, el cual no se ajusta al modelo de gas ideal.
Como podemos notar, es un concepto simple, pero de gran relevancia para estudios de termodinámica e ingeniería. Podemos considerar a un gas como real cuando éste se encuentre a presiones moderadas, o presiones elevadas y a bajas temperaturas. Esto quiere decir que el gas debe tener una densidad alta. Asimismo, para utilizar un modelo de gas real, el gas a estudiar debe encontrarse cerca del punto crítico, cerca del punto de condensación y a presiones elevadas.
Comportamiento de un gas real o no ideal
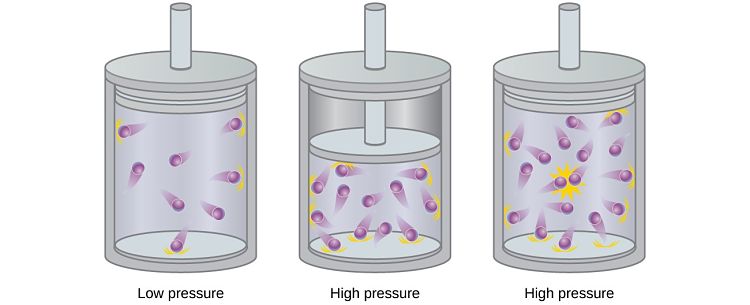 |
| Comportamiento de un gas a medida que aumenta la presión. Imagen de courseslumenlearning |
Las fuerzas atractivas entre las moléculas de un gas (fuerzas intermoleculares), junto a las fuerzas repulsivas a las cuales las moléculas del gas están expuestas, dan origen a que los gases se comporten de manera diferente a los gases ideal a presiones altas y bajas temperaturas. Este comportamiento se aleja del comportamiento ideal, a medida que se aumenta la presión o se baja la temperatura.
Así, en todos aquellos gases cuyas moléculas se encuentran sometidas a fuerzas intermoleculares (atracción y repulsión) a altas temperaturas y presiones bajas, el efecto de dichas fuerzas puede ser despreciado, por lo tanto, el gas sería ideal. A medida que la presión aumenta y la temperatura baja, estos efectos ya no podrán despreciarse, observándose una desviación de la idealidad, siendo necesario recurrir a modelos de gas real para poder estimar las propiedades termodinámicas con mayor confiabilidad.
Hay que destacar, que un gas real no se expande de manera infinita, ya que llega un momento en el cual el gas ya no se encontrará en la capacidad de ocupar más volumen, debido a la aparición de las fuerzas de Van der Waals entre sus moléculas.
¿Cuándo difiere un gas real de un gas ideal?
Con el objetivo de simplificar cálculos, se suele utilizar el modelo de gas ideal para realizar estimaciones en el estudio de gases o para trabajar con ellos, no obstante, utilizar esta aproximación en muchas oportunidades nos lleva a arrastrar un error considerable, sobre todo, cuando el sistema se encuentra a altas presiones, cerca del punto crítico o cerca del punto de condensación. Cuando el gas se encuentra en las proximidades de estos puntos, ya presenta una desviación considerable del comportamiento de gas ideal.
Asimismo, al contrario que con los gases ideales, para un gas real se deben considerar:
- Las fuerzas de Van der Waals.
- El efecto de compresibilidad.
- La capacidad calorífica.
- La composición variable del gas.
- Las reacciones químicas a las cuales están expuestos los gases.
- Los efectos termodinámicos de no equilibrio.
Podemos decir entonces, que un gas real comienza a diferir en su comportamiento de un gas ideal, cuando la presión a la que se encuentra se considera moderada o alta, ya que se hacen más evidentes y menos despreciables los efectos antes enumerados.
Factor de compresibilidad de un gas (Z)
 |
| Diagramas para estimar el factor de compresibilidad de un gas (Z). Imagen de chegg |
La desviación al comportamiento de gas ideal, puede ser cuantificada utilizando el concepto de factor de compresibilidad de un gas (Z), el cual, es un ajuste matemático que permite corregir la ecuación de gas ideal.
El factor de compresibilidad es un factor adimensional que se adiciona a la ecuación de gas ideal de la siguiente manera:
Donde:
- P: Presión a la cual se encuentra el gas.
- V: Volumen ocupado por el gas.
- n: Número de moles del gas.
- R: Constante general de los gases.
- T: Temperatura a la cual se encuentra el gas.
- Z: Factor de compresibilidad del gas.
El factor de compresibilidad de un gas se encuentra en valores comprendidos entre 0 y 1, siendo 1 el valor que representa la idealidad y los valores entre el 1 y el 0, representan las desviaciones del gas respecto a la idealidad. Mientras más cerca de 0 se encuentre el valor, más alejado de la idealidad estará el gas.
El factor de compresibilidad suele encontrarse en gráficas de Z en función de P en una gran cantidad de libros, como parte de la bibliografía tradicional de termodinámica. También, puede estimarse de manera algebraica utilizando funciones que dependen de la presión y la temperatura del gas, expresándose de la siguiente manera:
Se puede concluir, que para estimar el factor de compresibilidad de un gas se pueden utilizar gráficos termodinámicos levantados mediante datos experimentales, y que se ajustan bastante bien a la realidad, eso sí, hay que buscar gráficas de los gases que estamos estudiando, o de gases muy similares en estructura molecular. En este último caso, hay que considerar el error asociado al utilizar la aproximación a otro tipo de gas.
También pueden utilizarse las ecuaciones de estado, de las cuales hay muchas (cúbicas y generalizadas) y que se ajustan a diferentes tipos de condiciones de estudio e industriales. La selección de la ecuación dependerá de los requerimientos del cálculo y de las consideraciones tomadas en cuenta por el investigador o el ingeniero. Asimismo, el uso de este tipo de ecuaciones se debe complementar con un método numérico que facilite los cálculos, sobre todo, cuando estemos frente a una enorme cantidad de datos.

Gas real y factor de compresibilidad by Ing. Bulmaro Noguera is licensed under a Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional License











2 Comentarios
Muy útil, gracias.
ResponderBorrarGracias por tu comentario!
Borrar