La primera ley de la Termodinámica es una de las leyes fundamentales de la física y de la ingeniería química. Esta ley establece la relación entre el calor, el trabajo y la energía en un sistema termodinámico cerrado.
 |
| La primera ley de la Termodinámica y los principios de la energía |
En este artículo, explicaremos en detalle qué es la primera ley de la Termodinámica, cómo se aplica en la ingeniería química y cómo se puede utilizar en el diseño de procesos y en el análisis de sistemas energéticos. También, veremos la fórmula de la primera ley y cómo se puede aplicar para resolver problemas prácticos.
Tabla de Contenidos
- ✔¿Qué es la primera ley de la Termodinámica?
- ✔Definición de la primera ley de la termodinámica
- ✔Explicación de la primera ley de la termodinámica
- ✔Fórmula de la primera ley de la termodinámica
- ✔¿Cómo se aplica la primera ley de la Termodinámica en la ingeniería química?
- ✔Por qué es importante entender la primera ley de la Termodinámica en la ingeniería química?
- ✔La eficiencia energética en la ingeniería química
- ✔¿Cómo afecta la primera ley de la Termodinámica a la eficiencia energética en la ingeniería química?
- ✔Aplicación de la primera ley de la termodinámica en la industria
- ✔Ejercicios explicativos de la primera ley de la termodinámica
¿Qué es la primera ley de la Termodinámica?
 |
| Imagen que explica la primera ley de la Termodinámica con un cilindro pistón. Imagen de chemestrylearner |
La primera ley de la Termodinámica es un principio fundamental en la física y la ingeniería química que establece que la energía no se puede crear ni destruir, solo se puede transformar de una forma a otra. Este principio también se conoce como el principio de conservación de la energía, o primer principio de la termodinámica.
Es uno de los conceptos fundamentales en la Termodinámica, ya que nos permite entender cómo funciona la energía, lo que la convierte en teoría vital para los procesos industriales.
Definición de la primera ley de la termodinámica
La primera ley de la Termodinámica establece que:
La energía total en un sistema aislado permanece constante.
Es decir, la energía no se puede crear ni destruir, solo se puede transformar. Esto significa que la cantidad total de energía en un sistema cerrado (un sistema que no intercambia materia o energía con su entorno) permanece constante.
La energía puede cambiar de una forma a otra, como energía térmica, energía mecánica o energía química, pero la cantidad total de energía siempre se mantiene igual.
Explicación de la primera ley de la termodinámica
La primera ley de la Termodinámica se puede explicar con el concepto de balance de energía. En un sistema cerrado, la cantidad total de energía se puede expresar como la suma de la energía interna, el trabajo realizado y el calor transferido. Si un sistema no realiza trabajo ni intercambia calor con su entorno, entonces la energía interna del sistema permanece constante.
La energía interna de un sistema incluye la energía cinética de las partículas que componen el sistema y la energía potencial que se almacena en las fuerzas de interacción entre las partículas. Cuando se aplica una fuerza a un sistema cerrado, se realiza trabajo y la energía interna del sistema cambia. Si se transfiere calor al sistema, su energía interna también cambia. Esto lo podemos ver más claramente en la figura anterior, donde se puede ver que al adicionar calor al cilindro pistón (sistema cerrado), el volumen del gas se expande, generando un trabajo que va fuera del sistema, manteniendo la energía constante dentro del cilindro pistón.
Fórmula de la primera ley de la termodinámica
La primera ley de la Termodinámica se puede expresar matemáticamente como:
Donde:
- ΔU: Es el cambio en la energía interna del sistema
- Q: Es el calor transferido al sistema
- W: Es el trabajo realizado por el sistema
Ejemplos de primera ley de la termodinámica
A continuación, veremos algunos ejemplos que ilustran la primera ley de la termodinámica:
- Calentamiento de agua: Un ejemplo común de la primera ley de la termodinámica es el calentamiento de agua en una caldera. Cuando se agrega calor a la caldera, la energía térmica se convierte en energía interna del agua, lo que resulta en un aumento de la temperatura.
- Ciclo de refrigeración: Otro ejemplo de la primera ley de la termodinámica es el ciclo de refrigeración. En este ciclo, se utiliza energía para extraer calor de un espacio cerrado, lo que resulta en una disminución de la temperatura en el espacio cerrado.
- Otro ejemplo de la aplicación de la primera ley de la termodinámica es el cálculo de la energía liberada o absorbida durante una reacción química. La energía liberada o absorbida se puede calcular utilizando la variación de la entalpía del sistema.
Cómo se aplica la primera ley de la Termodinámica en la ingeniería química
 |
| Ecuación de la primera ley de la Termodinámica. Imagen de lawofthermodynamicsinfo |
En la ingeniería química, la primera ley de la Termodinámica es crucial para entender cómo la energía se transfiere y se transforma durante los procesos químicos. A continuación, analizaremos cómo se aplica la primera ley en la ingeniería química, por qué es importante entenderla y cómo se puede utilizar para el balance de energía en los procesos químicos.
EL primer principio de la Termodinámica se aplica en la evaluación de los procesos químicos y en la ejecución del balance de energía. El balance de energía es un concepto clave en la ingeniería química, que se utiliza para garantizar que la energía total que entra en un sistema sea igual a la energía total que sale del mismo.
En la práctica, esto se logra midiendo y evaluando la energía en diferentes etapas del proceso, incluyendo el trabajo, el calor y la entalpía. El trabajo es la energía transferida a través de una fuerza aplicada a un objeto, mientras que el calor es la energía transferida de un objeto a otro debido a la diferencia de temperatura. La entalpía es la cantidad total de energía en un sistema, incluyendo la energía interna y la energía asociada con la presión y el volumen del sistema.
¿Por qué es importante entender la primera ley de la Termodinámica en la ingeniería química?
La comprensión de esta ley de la Termodinámica es esencial para el estudio de los sistemas industriales, ya que permite a los ingenieros químicos diseñar y optimizar los procesos químicos de manera más eficiente. El balance de energía es fundamental en la evaluación y optimización de dichos procesos, lo que permite a los ingenieros químicos identificar y corregir problemas potenciales en el sistema o sistemas de trabajo.
Además, el primer principio de la Termodinámica es útil en la evaluación de la eficiencia energética de los procesos químicos. Al entender la cantidad de energía que entra y sale del sistema, los ingenieros químicos pueden identificar formas de reducir el consumo de energía y mejorar la eficiencia del proceso. Esto puede resultar en ahorros significativos de energía y costos para las empresas.
La eficiencia energética en la ingeniería química
La eficiencia energética en la ingeniería química es de vital importancia en la actualidad, debido a la creciente demanda de energía en todo el mundo y a la necesidad de reducir el impacto ambiental de la industria química. En este contexto, la aplicación de la primera ley de la Termodinámica es esencial para la optimización de los procesos químicos y procesos industriales en general.
¿Cómo afecta la primera ley de la Termodinámica a la eficiencia energética en la ingeniería química?
El primer principio de la termodinámica, también conocido como principio de conservación de la energía, es sumamente importante para el desarrollo de trabajos de ingeniería, ya que permite analizar el flujo de energía en los procesos químicos y establecer las condiciones óptimas para la transformación de esa energía.
La aplicación de la primera ley de la termodinámica en la ingeniería química se lleva a cabo mediante el análisis del balance de energía en los procesos químicos o industriales. Este análisis implica el estudio de los diferentes tipos de energía implicados en estos procesos, como la entalpía, la energía interna, el trabajo y el calor. A partir de estos datos, se puede determinar la eficiencia energética de un proceso químico y optimizar su diseño para minimizar la cantidad de energía perdida durante la transformación.
Aplicación de la primera ley de la termodinámica en la industria
La aplicación de la primera ley de la termodinámica en la industria química se encuentra orientada a reducir los costos de producción, para lograrlo se apoya en un aprovechamiento óptimo de la energía que se encuentra presente en los sistemas en estudio. Por ejemplo, en la producción de productos químicos a partir de materias primas, se puede optimizar el diseño del proceso para minimizar la cantidad de energía necesaria para llevar a cabo la reacción química. Además, se pueden implementar sistemas de recuperación de energía para aprovechar la energía que, de otro modo, se perdería durante el proceso.
Ejercicios explicativos de la primera ley de la termodinámica
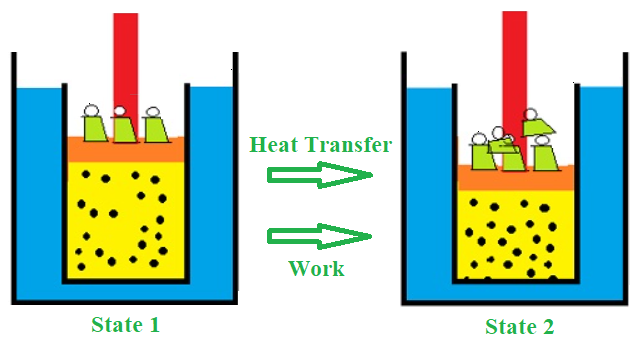 |
| Variación de un estado termodinámico conservando la energía interna. Imagen de overallscience |
A continuación, desarrollaremos un par de ejercicios para poder entender la primera ley de la termodinámica.
Ejercicio 1
Supongamos que tenemos un sistema cerrado que contiene 2 kg de agua líquida a 20°C. El sistema recibe una cantidad de calor de 1000 J y realiza un trabajo de 500 J sobre su entorno. ¿Cuál es el cambio en la energía interna del sistema, ∆U, durante el proceso?
Solución:
Primero, recordemos la expresión matemática de la primera ley de la termodinámica:
En este caso, la variación de energía interna del sistema (ΔU) será igual a la cantidad de calor que recibe el sistema (Q) menos el trabajo que realiza el sistema (W). Para resolver este problema, necesitamos conocer la cantidad de calor Q y el trabajo W, involucrados en el proceso.
La cantidad de calor Q que se transfiere al sistema es 1000 J. Para calcular el trabajo realizado por el sistema, necesitamos conocer el cambio en el volumen del sistema. En este caso, el agua se encuentra en un estado líquido, por lo que no hay un cambio significativo en el volumen.
Por lo tanto, podemos asumir que el trabajo realizado por el sistema es cero, es decir, W = 0. Ahora podemos calcular el cambio en la energía interna del sistema utilizando la ecuación:
Por lo tanto, el cambio en la energía interna del sistema es de 1000 J.
Ejercicio 2
Se tiene un sistema cerrado de volumen constante que contiene una cantidad determinada de gas ideal. El gas se encuentra inicialmente a una temperatura T1 y una presión P1. Durante un proceso, se transfiere una cantidad de calor Q al gas, y el gas realiza un trabajo W sobre su entorno. ¿Cuál es el cambio en la energía interna del gas, ∆U, durante el proceso?
Solución:
Primero, vamos a utilizar la ecuación de la primera ley de la termodinámica:
Al igual que en el ejercicio anterior, la variación de energía interna del gas (ΔU) será igual a la cantidad de calor que recibe el sistema (Q), menos el trabajo que realiza el sistema (W).
El trabajo realizado por el gas durante el proceso puede ser calculado como:
Donde:
- P1 es la presión inicial del gas
- ∆V es el cambio en el volumen del gas durante el proceso
En este caso, sin embargo, el volumen del sistema es constante, por lo que ∆V es cero, y el trabajo realizado por el gas es también cero: W = 0. Ahora, necesitamos determinar la cantidad de calor Q que se transfiere al sistema. Según la ley de conservación de la energía, la cantidad de calor transferida a un sistema es igual a la cantidad de trabajo que el sistema realiza sobre su entorno, más cualquier cambio en la energía interna del sistema. Por lo tanto, podemos escribir:
Donde:
- W es el trabajo realizado por el sistema
- ∆U es el cambio en la energía interna del sistema
Como ya hemos determinado que W es cero, podemos simplificar esta ecuación a:
Por lo tanto, la cantidad de calor Q que se transfiere al gas es igual al cambio en la energía interna del gas durante el proceso. Ahora, podemos calcular el cambio en la energía interna del gas utilizando la ecuación:
Donde:
- Cv es la capacidad calorífica a volumen constante del gas
- ∆T es el cambio en la temperatura del gas durante el proceso
Para un gas ideal monoatómico, la capacidad calorífica a volumen constante es igual a 3/2R, donde R es la constante universal de los gases. Por lo tanto, podemos escribir:
La primera ley de la Termodinámica explicada: Cómo la ingeniería química utiliza los principios de la energía by Ing. Bulmaro Noguera is licensed under a Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional License
















0 Comentarios